| 3.4.3. "Analyse und Synthese" in der Organischen Chemie - am Beispiel der Carbonsäureester |
|
Übersicht
|
||||||||||||||
0. Didaktische Anmerkungen für den Workshop Anhand der Synthese von Carbonsäureestern aus Alkoholen und Essigsäureanhydrid soll exemplarisch die Denk- und Arbeitsweise in der Organischen Chemie herausgearbeitet werden. Die Reaktion von Alkohol mit Carbonsäure ist eine enorm wichtige chemische Reaktion in der Biochemie und organischen Synthese. Die sogenannte Veresterung wird deshalb im Chemieunterricht das Experiment mit Ethanol und Essigsäure in einer einseitig offenen Apparatur (ohne Abzug) durchgeführt. Dabei wird der Essigsäureethylester gebildet, der Schülerinnen und Schülern vom Geruch her als Lösemittel für z.B. Nagellack oder Klebstoffen bekannt ist. Aber auch die Umkehrreaktion, die Verseifung, die Hydrolyse von Estern hat eine große Bedeutung. Das Experiment wird gemeinhin als gering gefährdend eingestuft und daher gern in Schülerübungen durchgeführt. Die auftretenden Edukte und Produkte sind als nur gering gefährlich anzusehen. Auch die zur Katalyse verwendete konzentrierte Schwefelsäure wird wegen seiner großen Verdünnung nicht als bedeutende Gefährdung erachtet. Das Experiment ist jedoch durch auftretende und nachweisbare Zwischenprodukte (hier Diethylsulfat Aus Furcht vor der Gefährdung die Estersynthese nur als Lehrerdemonstrationsexperiment oder gar nur Filmmaterial zu zeigen, vergibt eine Chance, an diesem wenig aufwändigen Experiment die grundlegenden Denk- und Arbeitsweisen zu vermitteln. Dazu gehören die Analyse durch Siedetemperaturbestimmung, die Synthese durch Vereinigen, Erhitzen unter Rückfluss mit Katalysator und die Trennung durch Destillation und Reinigung.
| ||||||||||||||
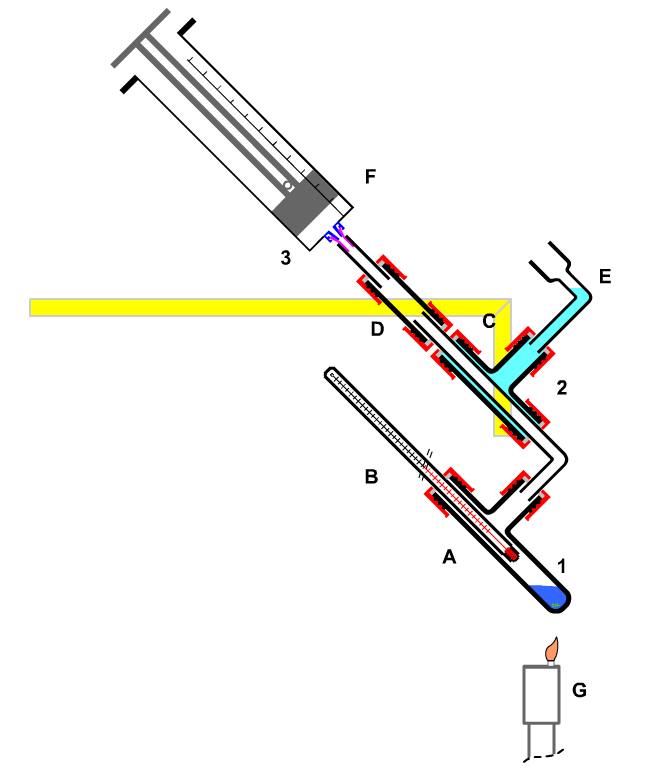
1. Das Experiment: Siedetemperaturbestimmung von Alkoholen Zunächst soll eine Apparatur entwickelt werden, die es erlaubt, die Siedetemperatur einer unbekannten, möglicherweise giftigen Flüssigkeit bei Normaldruck zu bestimmen.
Für die Konstruktion von Apparaturen gelten allgemeine Regeln.
Auszug für den Zusammenbau der Apparatur H aus Bild 1:
|
||||||||||||||
2. Didaktik: Systematische, schrittweise Konstruktion der Apparatur aus halbmikrotechnischen Geräten Ausführliche didaktische Diskussion Kurzfassung für die "Lehrerübung"
|
||||||||||||||
|
||||||||||||||
3. Chemische Operationen und Methoden für die Synthese Es gelten die allgemeinen Grundsätze für stoffliche Gleichgewichte.
Um chemische Reaktionen am Menschen zu vermeiden, dürfen Chemikalien nicht mit dem Menschen in Kontakt kommen. Dazu dienen die persönlichen Schutzmaßnahmen, Schutzbrille, Handschuhe und Brille. Sie sind allesamt redundante Sicherheitsmaßnahmen. Die primäre Schutzmaßnahme ist die geschlossene Apparatur. Genaues regelt die Gefahrstoffverordnung mit ihrem Schutzstufenkonzept Eine geschlossenen Apparatur muss aber auch gefüllt und entleert werden. Damit dabei aber keine gesundheitsgefährdenden oder giftigen Stoffe frei werden, wird ein Abzug benötigt. Der Abzug ist kein Teil der Apparatur! Um eine Apparatur zu konstruieren, geht man von den Aggregatzuständen der Edukte und erwarteten Produkte aus und kombiniert diese mit den Reaktionsbedingungen. Durch die Gefährlichkeit der Stoffe wird die Schutzstufe (Gefahrstoffverordnung) im Umgang mit den Stoffen bestimmt. Da hier bei den zu analysierenden Flüssigkeiten auch Methanol vorliegen kann, gilt: bei unbekannten Stoffe die Schutzstufe 3 (geschlossene Apparatur). Die Größe der Apparaturen hängt davon ab, wie viel Ausgangssubstanz vorhanden ist oder wie viel Produkt benötigt wird. Für analytische Zwecke, wie hier, werden möglichst kleine Stoffportionen eingesetzt. Für die Siedetemperaturbestimmung reichen bei dieser Apparatur 7 Tropfen Flüssigkeit. Wenn man ein Gemisch aus zwei Flüssigkeiten miteinander reagieren lassen will, benötigt man ein Gefäß. Wenn dabei Dämpfe entstehen, die gefährlich sein könnten, muss mit einem geschlossene Gefäß gearbeitet werden. Wenn die Reaktion durch Erhitzen gefördert werden soll, müssen für die entstehenden Gase Reserve-Volumen in der Apparatur bereitgehalten werden. Damit die Stoffe sich nicht als Gas dem Reaktionsbereich entziehen, müssen sie kondensiert und wieder zurückfließen können. Nach der Reaktion müssen die Edukte und Produkte getrennt werden. Haben die Edukte und Produkte unterschiedliche Siedetemperaturen, kann man die entstehenden Gase nach ihrer Kondensation in eine Vorlage ableiten. Damit unterscheiden sich Siedetemperaturbestimmung, Sieden unter Rückfluss und Destillation nur durch die Fließrichtung der kondensierten Stoffe. Bei geschickter Konstruktion der Apparatur können die drei Apparaturen ineinander überführt werden, ohne die Apparatur zwischenzeitlich, außer zum Füllen, zu öffnen. Für die Lage eines chemischen Gleichgewichtes gilt das "Prinzip des kleinsten Zwanges": Erhitzen beschleunigt die chemische Umsetzung, Kühlen verlangsamt sie. Exergonische Reaktionen werden durch Energiezufuhr zu geringeren Umsätzen verschoben und umgekehrt.
|
||||||||||||||
4. Durchführung und "gute Laborpraxis" Die Durchführung von Experimenten folgt grundlegenden Regeln, die in Form von Methoden (wiederkehrende Handlungsweisen) beschreibbar sind. Diese müssen auf den jeweils speziellen Fall zugeschnitten werden und nötigenfalls ergänzt werden, sofern sich neue grundlegende Erkenntnisse ergeben (Beispiel Umgang mit radioaktiven Stoffen und radioaktiver Strahlung). Im Folgenden sind einige allgemeine Regeln zusammengefasst. Methode: Gute Laborpraxis Methode: Leitregeln für den Umgang mit Gefahrstoffen Für die Konstruktion einer chemischen Apparatur gelten die Grundregeln der Stofftrennung und Stoffvereinigung. "Stoffe mit unterschiedlichem Reaktionsverhalten müssen vor unbeabsichtigtem Kontakt durch Puffervolumina getrennt sein". Zur Synthese wird der "leichter bewegliche" Stoff wird zum schwerer beweglichen Stoff hin bewegt. Für die Analyse wird der "schwerer bewegliche" Stoff zuerst entfernt.
|
||||||||||||||
5. Experiment: Essigsäureethylester aus Ethanol und Acetanhydrid mit Katalysator Schwefelsäure Die Apparatur zur Siedetemperaturbestimmung wird nach dem Erkalten geöffnet. Das Kühlwasser wird gegebenenfalls erneuert. 1 mL Ethanol und 2,5 mL Essigsäureanhydrid werden zusammen mit einem ausgeglühten, kalten Siedestein eingefüllt. Die Apparatur wird verschlossen und geneigt aufgestellt, damit das Kondensat zurückfließen kann. Mit einer Kerzenflamme (Teelicht) wird das Reaktionsgemisch erhitzt. Dabei muss die Spitze der Flamme mindestens 1 cm vom Boden des Reaktionsgefäßes entfernt bleiben. Durch Verändern des Abstandes der Flamme kann das Sieden so eingestellt werden, dass die Siedekrone noch unterhalb des Rückflusskühlers bleibt. Das Sieden wird ca. 10-15 Minuten aufrecht erhalten.
|
||||||||||||||
|
|
6. Stofftrennung durch Destillation und Sublimation Zum Destillieren wird der Kühler um 180° nach unten gedreht und das Ausgleichsgefäß entsprechend nach oben. Das Heizen sollte dabei nur ganz kurz unterbrochen werden. Damit die geringe Wärmeabgabe einer Kerzenflamme zum Übertritt des Dampfes in den Kühler ausreicht, ist es hilfreich, den seitlichen Ausgang bis zum Kühler mit Alufolie vor Wärmeabstrahlung zu schützen.
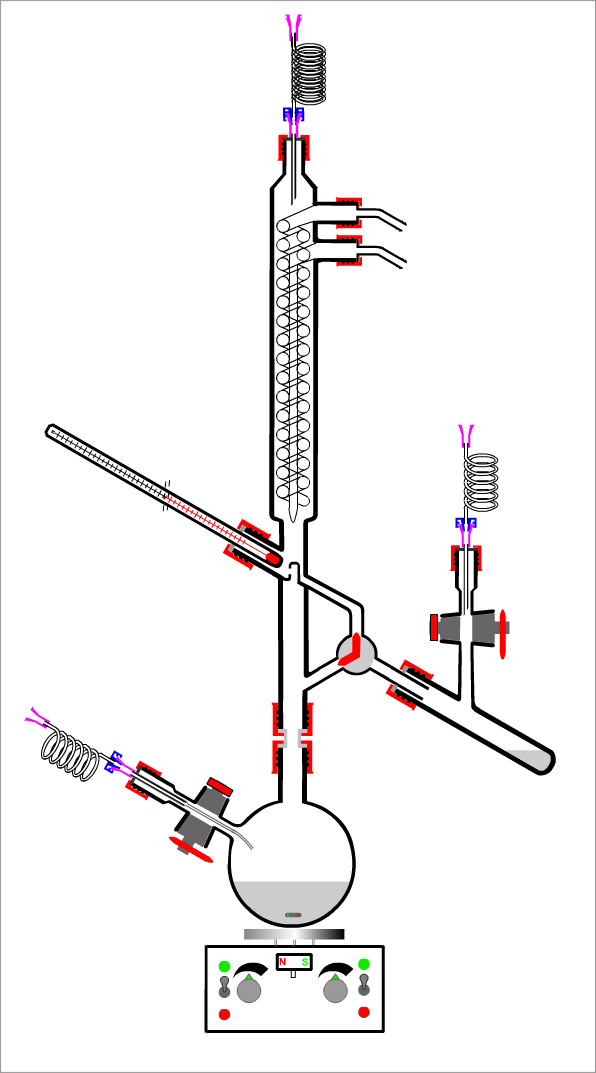
Stofftrennung durch fraktionierte Destillation Die fraktionierte Destillation wird angewendet, wenn drei oder mehr flüssige Stoffe zu trennen sind. Zwangsweise liegen bei mehreren Stoffen die Siedetemperaturen dichter beieinander. Da es sich bei der Destillation streng genommen um einen adiabtischen Vorgang handelt, sind Trennkolonnen hilfreich. Die bekannteste ist die sogenannte Vigreux-Kolonne (Art. 2479). Die nacheinander überdestillierenden Teile des Gemisches, "Fraktionen", werden mit Hilfe von Fraktionssammlern aufgefangen. Häufig wird dafür eine "Spinne" (Art. 2482; Skizze, Foto) eingesetzt, an die mehrere Vorlagen angeschlossen sind. Überlappen sich die Siedebereiche, weil viele Stoffe im Gemisch enthalten sind, werden Glockenboden-Kolonnen einsetzt (Beispiel Erdöl).
Stofftrennung durch "Vakuum"-Destillation Bei den kleinen Stoffportionen der Halbmikrotechnik kann man das Destillieren durch Anlegen eines Unterdrucks erreichen. Dazu braucht man nur am Stempel des Kolbenprober zu ziehen, der als Reservevolumen eingebaut ist. In der präparativen Chemie wird stattdessen ein Dauervakuum mittels Vakuumpumpe angelegt.
Stofftrennung durch Wasserdampfdestillation Liegt der abzutrennende Stoff im Gemisch als wasserunlöslicher Stoff vor, so wird häufig eine Wasserdampfdestillation eingesetzt. Streng genommen wird nur Wasser als mobile Phase "Transportmittel" eingesetzt, das bei dieser Temperatur die Stoffe mit niedrigem Dampfdruck mitreißt. Da Wasser bei 100°C siedet, liegen schonende Bedingungen vor, weshalb man viele pflanzlichen Inhaltsstoffe auf diese Weise gewinnt (Beispiel ätherische Öle). Stofftrennung durch Sublimation Ist es möglich, einen Stoff durch Sublimation abzutrennen, wird mit häufig mit einem "Fingerkühler" gearbeitet, da der sublimierte Stoff fest vorliegt und sich deswegen nicht leicht vom Trennort entfernt. Außenkühler - Innenkühler http://de.wikipedia.org/wiki/Labork%C3%BChler Rückfluss-Kühler http://de.wikipedia.org/wiki/R%C3%BCckflussk%C3%BChler
|
|||||||||||||
7. Stofftrennung durch Extraktion und "Scheiden"
Die Trennmethode des Extrahierens und Scheidens setzt zwei, nach Möglichkeit nicht mischbare, flüssige Phasen voraus. Beliebtes Lösemittel ist Wasser oder Benzin. Oftmals kann man die Unlöslichkeit eines abzutrennenden Stoffen in Wasser dadurch erhöhen, indem man die dem Wasser ein Salz zusetzt. Dadurch wird die Dipolwirkung durch die enthaltenen Ionen verstärkt. So lösen sich Ether, Ester oder Amine merklich in Wasser, die Löslichkeit nimmt aber stark ab, wenn statt Wasser eine gesättigte Lösung von Natriumsulfat oder Natriumchlorid genommen wird. Man nennt diese Abtrennung "Scheiden durch Aussalzen".
|
||||||||||||||
8. Stofftrennung durch Umfällen und Filtration Feste Stoffe eines Gemisches werden durch Filtration entfernt. Auch hier nutzt man die unterschiedlichen Löslichkeit der Stoffe eines Gemisches zum Trennen aus. In diesem Fall wählt man ein Lösemittel benutzt, um einen darin löslichen Stoff von einem darin unlöslichen Stoff abzutrennen. Auf diese Weise werden Verunreinigungen durch wiederholtes Auflösen in der Hitze und Auskristallisieren in der Kälte entfernt.
|
||||||||||||||
9. Stoffidentifikation
Unter dem Titel "Didaktik der Organischen Chemie nach dem PIN-Konzept" existiert eine Unterrichtsreihe, die sich mit der Synthese und Analytik von Kohlenstoff, Wasserstoff, Sauerstoffverbindungen befasst. Die Reihe kann als propädeutisch für ein naturwissenschaftliches Studium angesehen werden und ist für die Sek II ausgelegt, vorrangig für Leistungskurse. Es gibt eine ausführliche Website Allerdings wird dabei das Arbeiten in geschlossenen Systemen nicht angesprochen. Wie hier gezeigt, lässt sich die Arbeitstechnik mit geeignetem Gerät leicht den erforderlichen Ansprüchen anpassen. Schwerer wiegen die Bedenken , mit der Reagenzlösung "Dichromat-Test" in Schülerübungen zu arbeiten (siehe Kaliumdichromat
| ||||||||||||||
Bild 1: Siedetemperaturbestimmung von Alkoholen Bild 2: Systematische Entwicklung einer Apparatur zum Erhitzen von Flüssigkeiten unter Luftabschluss Bild 3: Rückflussapparatur Bild 4: Destillationsapparatur Bild 5: Sieden unter Rückfluss mit Gegenstromkühler Bild 6: Destillation mit Gegenstromkühler, "Liebig-Kühler" Bild 7: Sieden unter Rückfluss mit Gegenstromkühler Bild 8: Destillation mit Gegenstromkühler, "Liebig-Kühler" Bild 9: Sieden unter Rückfluss und fraktionierte Destillation mit Glockenboden unter Schutzgas (Schlenk-Technik) Bild 10: Destillation mit Gegenstromkühler ("Liebig-Kühler") und Vakuum-Anschluss Bild 11: Extraktion und Scheiden
|
||||||||||||||