Musterprotokoll: Das naturwissenschaftliches Versuchsprotokoll
prot_physik_siedediagramm.htm 27.10.2011
Experiment zur Temperaturänderung beim Erhitzen von Eis bei konstanter Energiezufuhr
als Demonstration eines Versuchsprotokolls
Inhalt
Beobachtung der Temperaturänderung beim Erhitzen von Eis mit konstanter Energiezufuhr
zur Aufklärung der Aggregatzustandsänderungen
Man kann Eiswürfel in kalte
Getränke geben, dabei kühlt sich das Gemisch ab, - jedoch nie unter 0°C.
Man verbrennt sich mit heißem Wasserdampf von 100°C stärker als mit der gleichen Menge
kochendem Wasser.
Die Skala der Thermometer sind nach dem schwedischen Naturwissenschaftler Celsius so festgelegt,
dass die Schmelztemperatur von Eis 0°C und die Temperatur des siedenden Wassers 100°C
bedeuten.
Wann soll was, wo und wie gemacht werden?
|
|
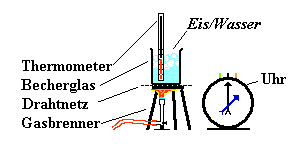
Stoffe:
Messgeräte:
Uhr mit Minuten- und
Sekundenzeiger
Thermometer -10 °C bis 150°C
- vor,
- während und
- nach dem eigentlichen Experiment?
Solange Wasser erhitzt wird, sollte am Experimentiertisch ein ganz dünner Wasserstrahl laufen, damit man sich im Falle einer Verbrennung oder Verbrühung schnell die Haut abkühlen kann. Sekunden sind hier wichtig!
In das Becherglas gibt man zur Vermeidung eines Siedeverzuges einen Siedestein ![]() .
.
dazu kommt noch der Siedestein (nicht in der Skizze dargestellt).
Bei Thermometern, die mit Alkohol gefüllt sind oder elektrisch messenden Thermometern, ist es zweckmäßig ein Kontrollthermometer mit Quecksilberfüllung (Lehrer) zusätzlich zu verwenden.
Die Anfangstemperatur wird abgelesen. Danach wird ein Gasbrenner mit rauschender Flamme unter das Becherglas mit Wasser gestellt. Unter fortwährendem Rühren wird in Abständen von 1 Minute die Temperatur gemessen und gemeinsam mit der Zeit in einer Tabelle notiert.
... und was kann er dabei beobachten?
| Nr. | Zeit (Minuten) | Temperatur (°C) | Bemerkung |
|---|---|---|---|
| 1 | 0 | 0 | Eis/Wasser |
| 2 | 1 | 0,5 | Eis/Wasser |
| 3 | 2 | 1 | Eis/Wasser |
| 4 | 3 | 5 | Wasser |
| 5 | 4 | 25 | Wasser |
| 6 | 5 | 45 | Wasser/ erste Blasen am Boden |
| 7 | 6 | 65 | Wasser/ Blasen am Rand |
| 8 | 7 | 85 | Wasser/ Blasen/ etwas Dampf über der Oberfläche |
| 9 | 8 | 97 | Wasser/ Blasen lösen sich vom Boden/ Dampf über der Wasseroberfläche |
| 10 | 9 | 100,5 | Wasser/ große Blasen lösen sich vom Boden und erreichen die Oberfläche/ deutlicher Wasserdampf über dem Becherglas |
| 11 | 10 | 100,5 | Wasser/ große Blasen lösen sich vom Boden und erreichen die Oberfläche/ deutlicher Wasserdampf über dem Becherglas |
| 12 | 11 | 100,5 | Wasser/ große Blasen lösen sich vom Boden und erreichen die Oberfläche/ deutlicher Wasserdampf über dem Becherglas |
Entfernt man den Brenner unter dem Becherglas, bevor sämtliches Wasser verdampft ist, kann man die Zeiten und Temperaturen in gleicher Weise aufnehmen. Das abgekühlte Wasser kann ins Abwasser gegeben werden. Der Siedestein gehört in den festen Hausmüll
Solange Eis vorhanden ist, steigt die Temperatur nicht an. Vermutlich dient die zugeführte Wärmeenergie dazu, die kleinsten Teilchen des Wassers aus dem Eiskristall herauszubrechen.
Nachdem das feste Eis geschmolzen ist, steigt die Temperatur an.
Wenn die Temperatur 100°C erreicht hat, bleibt die Temperatur unverändert und große Mengen Wasserdampf entweichen aus dem Becherglas. Offensichtlich wird die Flüssigkeit Wasser in gasförmiges Wasser umgewandelt. Die Temperatur im Becherglas steigt nicht weiter an, solange noch flüssiges Wasser vorhanden ist.
Bei Zufuhr von Energie durchläuft Wasser die
Aggregatzustände (festes) Eis, (flüssiges) Wasser und (gasförmiger) Wasserdampf, dabei
steigt die Temperatur im Wasser nicht.
Ist nur ein Aggregatzustand (Eis,
oder Wasser oder Dampf ) im Becherglas vorhanden , steigt die Temperatur nahezu
gleichmäßig an.
Beim Übergang von einem Aggregatzustand zu dem nächsten steigt die Temperatur nicht weiter an, statt dessen wird die Energie benötigt, um den Zusammenhalt des Stoffes zu aufzulösen.
Was bleibt zu tun?
Solange Eis/Wasser im gleichen Gefäß sind, ändert sich bei Entzug von Wärme nur der Eisanteil, er wird größer. Bei Zufuhr von Wärme nimmt der Wasseranteil im Gefäß auf Kosten des Eisanteils ab. Die Schmelztemperatur von Wasser verändert sich nicht. Auf diese Weise hat man den Nullpunkt der Celsius-Thermometerskala festgelegt.
Entsprechendes geschieht bei 100°C. Mit dieser Temperatur, bei der Wasser und Wasserdampf gleichzeitig vorhanden sind, legt man die zweite Temperatur der Celsius-Thermometerskala fest.
Ungeklärte Fragen:
- Werden beim Abkühlen (Entzug von Energie) die gleichen Temperaturen erreicht?
- Welchen Einfluss hat der Luftdruck auf den Versuch?
- Reagieren alle Feststoffe so auf das Erwärmen?
- Was geschieht bei der Erwärmung, wenn die Temperatur steigt? Wozu wird dabei Energie benötigt?
- Kann man die zugeführte Wärmeenergie zurückgewinnen?
- Wenn andere Stoffe andere Umwandlungstemperaturen hätten, könnte man daran die Stoffe erkennen, ohne sie dabei zu zerstören.
- Wenn man Lebensmittel kühlen möchte, kann sie in Eis legen. Sie bleiben solange auf 0°C gekühlt wie noch Eis da ist.
- Solange Wasser in einem Gefäß ist, kann beim Erhitzen das sich das Gefäß nicht wesentlich über 100°C erhitzen. Ist die letzte Flüssigkeit verdampft, kann das Gefäß und der Dampf jeder Temperatur erreichen, die die Energiequelle (Gasbrenner ca.800°C) vorgibt. Vorsicht daher beim Erhitzen von Glasgefäßen ohne Flüssigkeit, sie können platzen!
Autor (Text):
Copyright 2005-2015 HMTC Halbmikrotechnik Chemie GmbH; www.halbmikrotechnik.de