| 2. Zusammenhang mit physikalischen Erhaltungssätzen der Mechanik |
Energie-Erhaltungssatz und
Verständnis von Chemie
Klaus-G. Häusler
I. Das dynamische anorganische Gleichgewicht
II. Das biologische Fließgleichgewicht (in Vorbereitung)
| 1. Der Energie-Erhaltungssatz für die Anwendung im Fachbereich Chemie |
Es gelten drei Grundgesetze für ein chemisches Gleichgewicht, die eingeteilt sind nach den Prinzipien der Mechanik:
1. Trägheitsprinzip:
Anorganische Stoffe, die sich lange Zeit unter gleichen Bedingungen berühren, verharren in ihrem chemischen Zustand, solange keine Energie zugeführt oder entzogen wird. Dieser Zustand gilt als chemisch neutral.2. Aktionsprinzip
Wirkt man von außen auf Stoffe mit Energieänderung ein, so ändert sich die Temperatur, die Verteilung oder die chemische Zusammensetzung.
3. Reaktionsprinzip
Bilden sich in einem geschlossenen System neue Stoffe, dann ist ihre chemische Wirkung entgegengesetzt gleich groß.
Diese Sätze sind eine allgemeinverständliche Umformungen des 2. Hauptsatzes der Thermodynamik. Sie beschreiben den Energieerhaltungssatz unter Einbeziehung der chemischen Energie. Sie besitzen Gültigkeit für alle Stoffe und chemischen Reaktionen und beschreiben den Zustand eines natürlichen Gleichgewichtes der Stoffe mit ihrer Umgebung.
| 2. Zusammenhang mit physikalischen Erhaltungssätzen der Mechanik |
nach Galilei:
Die moderne exakte Wissenschaft begann mit der Feststellung Galileo Galileis (1564-1642), dass zur Aufrechterhaltung einer geradlinig gleichförmigen Bewegung keine Ursache nötig ist. Diese Feststellung entspricht dem ersten Grundsatz stabiler chemische Gleichgewichte.
nach Newton:
Isaac Newton (1643-1742) war nicht nur an der Beschreibung von Geschwindigkeitsgesetzmäßigkeiten, sondern an der an der Erforschung Ursachen gelegen war. Er erweiterte die Bewegungsbeschreibung eines Körpers zu den drei Grundprinzipien eines jeden Gleichgewichts, indem er als Ursache Kräfte einführte.
1. Trägheitsprinzip:
Ohne Einwirkung von Kraft verharrt ein Körper in seiner gleichförmig geradlinigen Bewegung.
2. Aktionsprinzip:
Wirkt auf einen beweglichen Körper eine Kraft ein, so ändert sich die Richtung und/oder die Geschwindigkeit seiner Bewegung.
(Newton formulierte das Aktionsprinzip viel genauer und unter Vorwegnahme der Relativitätstheorie unter Zuhilfenahme des Impulses).3. Reaktionsprinzip:
In einem geschlossenen System sind die Kräfte, die von den Körpern aufeinander einwirken, entgegengesetzt gleich.
Der Zusammenhang mit diesen Gesetzen für Kräfte und ihre Wirkung auf Körper ist in mehrerer Hinsicht vergleichbar mit den vorangestellten Gesetzen für Energien und ihre Wirkung auf Stoffe.
- Energien E sind physikalisch mit Kräften F verbunden: E = F * s, worin s den Weg bezeichnet, den ein Körper der Masse m in Richtung des Kraft durchläuft. In der Chemie ist anders als in der Physik die Richtungsabhängigkeit oder zurückgelegte Wege nicht von Bedeutung, wodurch die Ähnlichkeit der Gesetzmäßigkeiten noch augenfälliger wird.
- Kräfte können auch der Verformung von Körpern dienen. Dabei ändert sich natürlich auch die momentane Geschwindigkeit eines Teils des Körpers. In diesem Fall wird die Energie der Verformung als Spannungsenergie im Körper gespeichert, was der Anregungsenergie bei Stoffen entspricht.
- Einen Zustand, der keinerlei Wirkung auf seine Umgebung ausübt, bezeichnet man sowohl in der Physik als auch in der Chemie als neutral (elektrisch neutral, pH-neutral)
- Auch der Sprachgebrauch zeigt Parallelitäten, so spricht man
- bei chemisch reaktionsträgen Stoffen von inerten Stoffen (Trägheitssatz),
- bei Stoffen, die eine Wirkung besitzen von Agenzien (Aktionsprinzip) und
- bei Stoffen, die auf andere Stoffe reagieren, indem sie deren Eigenschaften neutralisieren von Reagenzien.
| 3. Was bedeutet der Begriff "Chemikalie" und "chemische Reaktion"? |
Unter Chemikalien versteht man Stoffe, die sich in ihrer Umgebung nicht im chemischen Gleichgewicht befinden.
Um Stoffe aus ihrem chemischen Gleichgewicht zu bringen, ist die Zufuhr von Energie notwendig. Es stehen verschiedene Energien zur Verfügung: Wärme, elektrische Energie, kinetische Energie, Kompressionsarbeit, um nur die wichtigsten zu nennen. Eine besondere Art der Energie ist die Konzentrationsänderung eines Stoffes am gleichen Ort. Eine einfache Art der Energiezufuhr ist die "Umverteilung". Sie kann darin bestehen, dass man den Stoff von seinem ursprünglichen Ort an einen anderen bringt, wo er mit anderen Stoffen in Kontakt kommt.
Diese umgangssprachliche Beschreibung des Zustandekommens einer chemischen Reaktion ist nichts anderes als der 2. Hauptsatzsatz der Thermodynamik.
mit
G Freie Enthalpie
H Enthalpie
T absolute Temperatur
S Entropie
Für Stoffe, die sich im Gleichgewicht mit ihrer Umgebung befinden, gilt:
,
für Chemikalien, gilt allgemein:
,
für exergonische Reaktionen gilt:
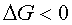
und für endergonische Reaktionen
.
Chemikalien besitzen die Eigenschaft, sich mit ihrer Umgebung ins Gleichgewicht zu setzen. Wenn sich dabei Stoffe mit anderer Zusammensetzung bilden, spricht man bei diesem Ausgleich mit der Umgebung von einer chemischer Reaktion. Nur die Exergonischen Reaktionen laufen freiwillig ab, endergonische Reaktionen muss man durch Energiezufuhr erzwingen.
| 4. Welche Aufgabe hat die chemische Forschung? |
Für den Chemieunterricht bietet das Voranstellen dieser Gesetze über chemische Gleichgewichte, eine Möglichkeit, die Herstellung, Untersuchung und Umsetzung mit anschließender "Entsorgung" von Chemikalien vorzunehmen.
Im Idealfall wird in der Schule aus einem Stoff, der sich in natürlichem chemischen Gleichgewicht mit der Umgebung befindet, durch Zufuhr von Energie in neue Stoffe aufgespalten. Die Aufnahme der zugeführten Energie führt zur Bildung neuer Stoffe, womit die Energie chemisch gespeichert ist. Diese neugebildeten Stoffe kann man jetzt als Chemikalien bezeichnen, da sie die Reaktionsfähigkeit besitzen mit anderen Stoffen erneute chemische Veränderungen zu durchlaufen.
In der wissenschaftlichen Chemie gilt es herauszufinden, worin die Gesetzmäßigkeiten der Spaltung der Stoffe und die Bildung neuer Stoffe bestehen. In der technisch-industriellen Chemie wird versucht durch die Bildung neuer Stoffe einen Einfluss auf die Umgebung des Menschen auszuüben, der vorteilhaft für das Leben des Menschen ist. Dazu muss sich der neugebildete Stoff in das natürliche Gleichgewicht einfügen. Als chemisches Endprodukt darf er keine wesentliche chemische Aktivität als Chemikalie entfalten. Als Wirkstoff (Agens) soll er dagegen die Umwelt verändern.
Die chemische Forschung soll Erkenntnisse sammeln, die es möglich machen, die Wirkung von Stoffen (Chemikalien) auf die Umwelt vorherzusagen, um gezielt gewünschte Veränderungen herbeizuführen oder um unerwünschten entgegenzuwirken.
| 5. Welche Aufgabe hat die Chemische Industrie? |
Aufgabe der Chemischen Industrie ist es, Stoffe in genügendem Umfang bereitzustellen, die dem Menschen für seine Existenz Vorteile verschaffen. Über die Bedeutung der Chemischen Industrie für die gesteigerte Lebenserwartung und den Komfort der Menschen in den Industriestaaten braucht nicht viel gesagt zu werden. Die Errungenschaften sind so gewichtig , dass kein Zweifel am Nutzen aufkommen kann.
Alle Fällen, in denen ein neuer Stoff in die Umwelt gebracht wird, ist wichtig, dass die Veränderungen, die die Anwendung des neuen Stoffes bringen, vorwiegend nützlich sind, mindestens jedoch nicht schädlich. Fast immer muss die Herstellung eines Stoffes an anderer Stelle als seine Verwendung stattfinden. In diesem Fall verlässt ein reaktiver Stoff das "Gelände der Chemischen Industrie", um an anderer Stelle weiterverarbeitet zu werden oder wie bei Düngemittel und Pestiziden verteilt zu werden.
An diesen Fällen wird deutlich, dass die Chemische Industrie eine Art Dienstleistung an der Gesellschaft erbringt, die nicht der Kritik durch die gleiche Gesellschaft unterliegen kann. Es ist auch nicht die Bereitstellung von Chemikalien, sondern der unsachgemäße Umgang mit Chemikalien, der der Gesellschaft insgesamt, auch den Naturwissenschaftlern wo auch immer, Sorgen macht.
Auch der Chemieunterricht profitiert von der Bereitstellung von Chemikalien durch die Industrie, indem Chemikalien, eine Art "Halbzeug", eingekauft und bereitgehalten werden, um chemische Sachverhalte vermitteln zu können. Insbesondere in der Schule wird man den Idealfall, von einem natürlichen Ausgangsstoff ausgehend, neue Stoffe herzustellen, zu untersuchen und sie wieder in den Ausgangstoff zurückzuführen, selten nutzen können. Dazu sind die Energien, die zur Bildung neuer Stoffe führen häufig zu groß. Wenn man bedenkt, dass bereits zur Stofftrennung und Reinigung oftmals erhebliche Mengen von Energie aufgewendet werden muss, versteht man, dass bereits Reinstoffe als Chemikalien eingestuft werden müssen, befinden sie sich doch in ihrer Konzentration nicht im natürlichen Gleichgewicht.
In der Schule ist das Endprodukt "Wissen", weitere Produkte der Produktion von Wissen sind Stoffe. Genau wie überall bei der Anwendung von Chemikalien sollten die Endprodukte keinen Anlass zur "Besorgnis" geben, wenn es in die Umgebung entlassen werden.
| 6 . Was bedeutet der Begriff "Entsorgung"? |
Von Chemikalien gehen um so mehr eine Gefahren aus, je weiter sie vom natürlichen Gleichgewicht der Umgebung entfernt sind. Man muss dann "Sorge haben", dass der schmale Bereich der natürlichen Lebensbedingungen verlassen wird.
Erst wenn die neugebildeten Stoffe sich wieder im natürlichen Gleichgewicht mit ihrer Umgebung befinden, gelten sie als chemisch neutral. Nach einer Abfolge von chemischen Reaktion müssen sich die Reaktionsprodukte im natürlichen Gleichgewicht mit der Umgebung befinden, wenn sie als "entsorgt" gelten sollen.
Für diese Überlegungen sind Schülerversuche zum natürlichen Kalk-Kreislauf und den technischen Produkte Kalksandstein und Mörtel von unterrichtlicher Bedeutung.
Schülerinnen und Schüler haben damit ein Kriterium für die Beurteilung verantwortungsbewusstes chemischen Handelns.
Der Unterschied "Entsorgen" und "zur Entsorgung bereitstellen"?
Ebenso, wie die Chemische Industrie Chemikalien im Auftrag der Gesellschaft herstellt und in Verkehr bringt, ist muss die Chemische Industrie der Gesellschaft bei der Entsorgung helfen. Auch hier kann der Energie-Erhaltungssatz und andere Erhaltungssätze Leitlinie bei der Entsorgung sein.
Bei der Entsorgung gilt es, einer Chemikalie ein geeignetes Reagenz (Antagonist, Gegenspieler) zuzugeben, das die Reaktivität zu einen Gleichgewicht ergänzt. Ein Blick auf die anorganische Chemie zeigt, dass im wesentlichen nur drei Arten von chemischen Reaktionen vorkommen:
Das Reagenz zur Entsorgung muss demnach ein Stoff sein, der selbst in den natürlichen Gleichgewichten vorkommt, damit das Reagenz, auch im Überschuss angewendet, nicht selbst ein gefährlicher Stoff ist. Außerdem muss das Reagenz die geeignete antagonistische Reaktion zur der zu entsorgenden Chemikalie zeigen. Geeignet sind:
Wie erkennt, gehört zur planvollen Entwicklung einer "Entsorgungs-Industrie" ein Grundwissen über die Eigenschaften von Chemikalien, das komplementär zum Wissen über die Herstellung von Chemikalien ist.
Im Chemieunterricht muss die Entsorgung Bestandteil der Betrachtung einer chemische Reaktion sein. Ziel ist es bei der Entsorgung ein anorganisches dynamische Gleichgewicht zu erreichen, das dem natürlichen chemischen Gleichgewicht nahe kommt.
Wenn es nicht möglich ist, im Experiment die Gefahrstoffe zu entsorgen, müssen die Gefährlichen Stoffe "zur Entsorgung bereitgestellt werde". Das geschieht in Absprache mit den örtlichen Entsorgungsunternehmen, die je nach ihren Entsorgungstechniken spezielle Regeln für die Sammlung der zu entsorgenden Stoffe erarbeitet haben und geeignete Gefäße bereitstellen. Der Laie darf keine "Entsorgung" vornehmen. Hierfür verfügen die Kommunen zum Teil mobile Sondermüll-Fahrzeuge, bei denen die gefährlichen Stoffe abgegeben werden können.
Autor (Text): Klaus-G. Häusler;
![]() haeusler[at]muenster[dot]de
haeusler[at]muenster[dot]de
Bearbeitung (WWW): Klaus-G. Häusler
Literatur:
© 1997-2001 HMC - Halbmikrotechnik Chemie;
Klaus-G. Häusler; ![]() haeusler[at]muenster[dot]de
haeusler[at]muenster[dot]de
uiw/fach/chemie/inhalt/didaktik/inhalt/erhltg.htm
09.09.04